Cetoconazol
| Cetoconazol Alerta sobre risco à saúde | |
|---|---|
| |

| |

| |
| Identificadores | |
| Número CAS | |
| PubChem | |
| DrugBank | APRD00401 |
| ChemSpider | |
| Código ATC | J02 |
| Propriedades | |
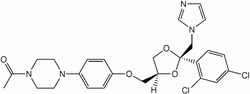
| Fórmula química | C26H28Cl2N4O4 |
| Massa molar | 531.41 g mol-1 |
| Ponto de fusão |
146 °C[1] |
| Solubilidade em água | praticamente insolúvel[2] |
| Farmacologia | |
| Biodisponibilidade | Variável |
| Via(s) de administração | Tópica |
| Metabolismo | Hepático |
| Meia-vida biológica | Bifásico: Fase inicial: 2 horas Fase terminal: 8 horas |
| Ligação plasmática | 84 a 99% |
| Excreção | Biliar e renal |
| Riscos na gravidez e lactação |
B3(AU) C (EUA) |
| Riscos associados | |
| Frases R | R60, R25, R48/22, R35 |
| Frases S | S53, S45, S60, S61 |
| LD50 | 166 mg·kg-1 (Rato, via oral) [1] |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Cetoconazol é um fármaco antimicótico ou antifúngico derivado do imidazol usado topicamente (creme, gel ou xampu). Descoberto na década de 1980. Na forma oral é mais tóxico que outros antifúngicos.
O cetoconazol, vendido sob a marca Nizoral entre outros, é um medicamento antiandrogénio, antifúngico e antiglicocorticóide usado para tratar uma série de infecções fúngicas.[3] Aplicado na pele, é usado para infecções fúngicas da pele como tinea, candidíase cutânea, pitiríase versicolor, caspa e dermatite seborreica.[4] A administração via oral é uma opção menos preferida e recomendada apenas para infecções graves quando outros agentes não podem ser usados.[3] Outros usos também incluem o tratamento do crescimento excessivo de pelos com padrão masculino em mulheres e síndrome de Cushing.[3]
Os efeitos colaterais comuns quando aplicado na pele incluem vermelhidão.[4] Os efeitos colaterais comuns quando tomados por via oral incluem náuseas, dor de cabeça, e problemas hepáticos.[3] Os problemas hepáticos podem resultar em morte ou na necessidade de um transplante de fígado.[3][5] Outra causa grave dos efeitos quando tomado por via oral incluem prolongamento do intervalo QT, insuficiência adrenal e anafilaxia.[3][5] É um imidazol e atua impedindo a produção de ergosterol necessário para a membrana celular do fungo, retardando assim o crescimento.[3]
O cetoconazol foi patenteado em 1977 pela empresa farmacêutica belga Janssen, e entrou em uso médico em 1981.[6] Está disponível como medicamento genérico e as formulações aplicadas na pele estão isentos de prescrição médica no Reino Unido.[4] Em 2021, foi o 161º medicamento mais prescrito nos Estados Unidos, com mais de 3 milhões de prescrições.[7][8] A formulação tomada por via oral foi retirada na União Europeia e na Austrália em 2013,[9][10] e na China em 2015.[11] Por outro lado, o seu uso foi restringido nos Estados Unidos e no Canadá em 2013.[10]
Riscos na gravidez e bebé
editarO cetoconazol é classificado como categoria de gravidez C nos EUA.[12] O seu uso não é recomendado em bebés com menos de 2 anos de idade via oral.[13] Por não ser absorvido topicamente, não há contraindicação em nenhum dos casos.[14] Por via oral, apresentou alterações fetais em ratos, portanto o seu uso em gestantes ou lactantes não é recomendado.
Indicação
editarÉ usado em creme, gel ou champô de 1 a 2% para tratar:[15]
- Pé de atleta (tinea pedis);
- Micose corporal (tinea corporis);
- Micose da virilha (tinea cruris);
- Dermatite seborreica;
- Micose do sol (Tinea versicolor ou pitiríase versicolor);
- Candidíase cutânea
Tem acção antimicótica in vitro sobre os seguintes fungos: Blastomyces dermatitidis, Candida spp., Coccidioide immitis, Epidermophyton floccosum, Histoplasma capsulatum, Malassezia spp., Microsporum canis, Paracoccidioide brasiliensis, Trichophyton mentagrophytes e Trichophyton rubrum. É bastante eficaz, para pele.
Após o uso de corticosteróides tópicos, recomenda-se esperar duas semanas antes de prosseguir com o tratamento das mesmas áreas com cremes à base de cetoconazol.[14]
Efeitos colaterais
editarÉ incomum (4% dos usuários) que cause coceira, ardor, queimação, vermelhidão ou irritação no local onde foi aplicada. Mudar de medicamento se ocorrer. Também é incomum (1%) deixar a pele mais seca ou mais oleosa ou causar dor de cabeça. Outros efeitos colaterais são raros (menos de 1%). Como comprimido era hepatotóxico (15%) e causava problemas gastrointestinais (3%) por isso parou de ser usado.[16]
Referências
- ↑ a b (en) « Cetoconazol » em ChemIDplus
- ↑ Europäische Arzneibuch-Kommission, ed. (2006). «EUROPÄISCHE PHARMAKOPÖE 5. AUSGABE». 5.0–5.8
- ↑ a b c d e f g «Ketoconazole Monograph for Professionals». Drugs.com. American Society of Health-System Pharmacists. Consultado em 23 March 2019. Cópia arquivada em 28 December 2010 Verifique data em:
|acessodata=, |arquivodata=(ajuda) - ↑ a b c British national formulary : BNF 76 76 ed. [S.l.]: Pharmaceutical Press. 2018. 1198 páginas. ISBN 9780857113382
- ↑ a b «FDA limits usage of Nizoral (ketoconazole) oral tablets due to potentially fatal liver injury and risk of drug interactions and adrenal gland problems». FDA Drug Safety Communication. U.S. Food and Drug Administration. 26 July 2013. Consultado em 23 November 2013. Cópia arquivada em 2 December 2013 Verifique data em:
|acessodata=, |arquivodata=, |data=(ajuda) - ↑ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. [S.l.]: John Wiley & Sons. p. 503. ISBN 9783527607495
- ↑ «The Top 300 of 2021». ClinCalc. Consultado em 14 January 2024. Cópia arquivada em 15 January 2024 Verifique data em:
|acessodata=, |arquivodata=(ajuda) - ↑ «Ketoconazole - Drug Usage Statistics». ClinCalc. Consultado em 14 January 2024. Cópia arquivada em 8 July 2020 Verifique data em:
|acessodata=, |arquivodata=(ajuda) - ↑ «Oral ketoconazole (Nizoral) 200 mg tablets». Therapeutic Goods Administration (TGA). 10 October 2013. Consultado em 23 March 2019. Cópia arquivada em 2 July 2015 Verifique data em:
|acessodata=, |arquivodata=, |data=(ajuda) - ↑ a b Gupta AK, Lyons DC (2015). «The Rise and Fall of Oral Ketoconazole». Journal of Cutaneous Medicine and Surgery. 19 (4): 352–7. PMID 25775613. doi:10.1177/1203475415574970
- ↑ «国家食品药品监督管理总局关于停止生产销售使用酮康唑口服制剂的公告(2015年第85号)» (em chinês). China Food and Drug Administration. 25 June 2015. Consultado em 2 July 2015. Cópia arquivada em 2 July 2015 Verifique data em:
|acessodata=, |arquivodata=, |data=(ajuda) - ↑ «Ketoconazole (Nizoral) Use During Pregnancy». Drugs.com (em inglês). Consultado em 24 May 2020. Cópia arquivada em 10 April 2020 Verifique data em:
|acessodata=, |arquivodata=(ajuda) - ↑ Kazy Z, Puhó E, Czeizel AE (March 2005). «Population-based case-control study of oral ketoconazole treatment for birth outcomes». Congenital Anomalies. 45 (1): 5–8. PMID 15737124. doi:10.1111/j.1741-4520.2005.00053.x Verifique data em:
|data=(ajuda) - ↑ a b «Copia arquivada». Consultado em 1 de novembro de 2011. Cópia arquivada em 5 de março de 2016
- ↑ http://www.mayoclinic.org/drugs-supplements/ketoconazole-topical-route/description/drg-20067739
- ↑ http://www.mdsaude.com/2014/11/cetoconazol.html