Mirogabalina
| Mirogabalina Alerta sobre risco à saúde | |
|---|---|
| |
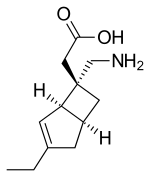
| Nome IUPAC | (1R,5S,6S)-6-(aminomethyl)-3-ethyl-bicyclo(3.2.0)hept-3-ene-6-acetic acid |
| Outros nomes | DS-5565 |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| Código ATC | N02 |
| SMILES |
|
| Primeiro nome comercial ou de referência | Tarlige |
| Propriedades | |
| Fórmula química | C12H19NO2 |
| Massa molar | 209.27 g mol-1 |
| Farmacologia | |
| Via(s) de administração | oral |
| Classificação legal |
Lista de substâncias sujeitas a controle especial - Lista (BR)
|
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Mirogabalina (nome comercial: Tarlige; código de desenvolvimento: DS-5565) é um gabapentinoide desenvolvido pela farmacêutica japonesa Daiichi Sankyo. Outros exemplos de gabapentinoides são a gabapentina e a pregabalina. Como gabapentinoide, a mirogabalina se liga à subunidade α2δ dos canais de cálcio dependentes de voltagem (1 e 2), mas possui potência significativamente maior quando comparada à pregabalina. A mirogabalina demonstrou bons resultados em ensaios clínicos de Fase II para tratamento da neuropatia diabética.[1][2]
Pesquisa e desenvolvimento
editarResultados de ensaios clínicos de Fase III:
- Eficaz: para neuralgia pós-herpética
- Ineficaz: para fibromialgia[3]
- Eficaz: para dor neuropática e neuropatia diabética[4]
Histórico
editarNo Japão, a farmacêutica Daiichi Sankyo apresentou um pedido de aprovação da mirogabalina para o tratamento da dor em casos de neuropatia periférica.[5] O medicamento foi aprovado para tratamento de dor neurogênica e neuralgia pós-herpética no Japão em janeiro de 2019.[6]
Referências
- ↑ Vinik A, Rosenstock J, Sharma U, Feins K, Hsu C, Merante D (dezembro de 2014). «Efficacy and safety of mirogabalin (DS-5565) for the treatment of diabetic peripheral neuropathic pain: a randomized, double-blind, placebo- and active comparator-controlled, adaptive proof-of-concept phase 2 study». Diabetes Care. 37: 3253–61. PMID 25231896. doi:10.2337/dc14-1044
- ↑ Vinik A, Sharma U, Feins K, Hsu C, Merante D (2014). «DS-5565 for the Treatment Of Diabetic Peripheral Neuropathic Pain: Randomized, Double-Blind, Placebo- And Active Comparator-Controlled Phase II Study (S20.004)». Neurology. 82: S20.004
- ↑ «Daiichi Sankyo Announces Top-line Results from Phase 3 Global Clinical Development Program Evaluating Mirogabalin in Pain Syndromes». Daiichi Sankyo. 30 de junho de 2017
- ↑ «Daiichi Sankyo Announces Positive Top-line Results from Phase 3 Clinical Trial Evaluating Mirogabalin in Diabetic Peripheral Neuropathic Pain». Daiichi Sankyo. 31 de agosto de 2017
- ↑ «Daiichi Sankyo Submits Marketing Application for Mirogabalin in Japan». Daiichi Sankyo. 15 de fevereiro de 2018
- ↑ https://adisinsight.springer.com/drugs/800033181
Ligações externas
editar- «Mirogabalin». Drug Information Portal. U.S. National Library of Medicine